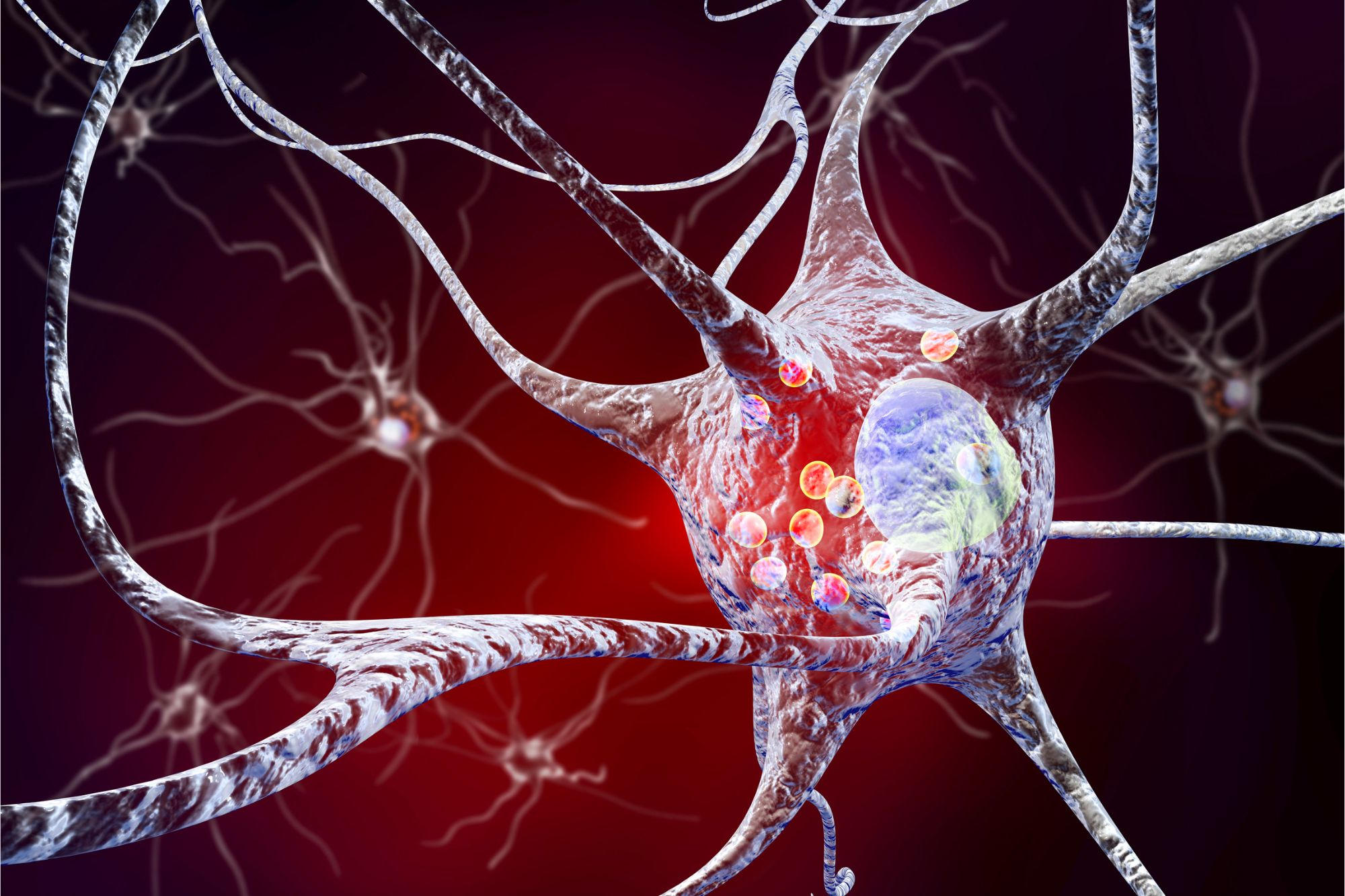
一項新的研究挑戰了長期以來的觀點:阿茲海默症主要是由澱粉樣斑塊驅動的,而不是指向神經元內部微妙但關鍵的競爭。
領導的新研究,顯示阿茲海默症可能不像人們普遍認為的那樣僅僅由大腦中斑塊的堆積引起。相反,它可能是由一種蛋白質破壞另一種蛋白質的正常功能引起的。
多年來,科學家一直將β澱粉樣蛋白(a-β)視為阿茲海默症的主要原因。這種蛋白質的簇常見於患者體內,而提高 a-β 水平的基因突變已知會引發早發性阿茲海默症。
然而,數以千計的旨在消除α-β的臨床試驗未能阻止或逆轉這種疾病。
研究人員也知道,另一種蛋白質 tau 蛋白會在阿茲海默症患者的大腦中累積。儘管如此,tau 蛋白和 a-beta 蛋白如何相互作用仍不確定。 「除了失智症之外,阿茲海默症的診斷還需要大腦中 a-beta 和 tau 蛋白的積累,」加州大學河濱分校化學教授兼研究主要作者 Ryan Julian 說。 “但許多實驗室只關注其中一個的作用而忽略另一個。”
這項新研究發表於美國國家科學院院刊顯示兩種蛋白質之間存在直接聯繫。
Tau 在穩定微管(細胞內結構)方面發揮關鍵作用。這些微小的管子就像運輸路線一樣,幫助在神經細胞中移動必需的分子。沒有它們,神經元就無法傳遞生存和溝通所需的物質。
神經元內部的競爭
研究團隊發現,tau 蛋白與微管結合的部分與 a-beta 的大小和形狀非常吻合。這種相似性表明 a-beta 也可能附著在這些結構上。
為了測試這一點,研究人員用螢光標記標記了 a-β。它的運動和光訊號的變化使他們能夠檢測到它何時與微管結合。
結果表明,a-β 和 tau 蛋白以相似的強度附著在微管上。這意味著當 a-beta 在神經元內部積聚時,它會將 tau 蛋白推離原來的位置。
Julian 說:“我們的工作表明,β 澱粉樣蛋白和 tau 蛋白會競爭微管上的相同結合位點,而 a-β 蛋白會阻止 tau 蛋白正常發揮作用。”
這種幹擾可能標誌著疾病的開始。當 tau 蛋白被取代時,細胞的內部運輸系統開始出現故障。同時,tau 蛋白可以開始聚集在一起並移動到神經元中不屬於它的部分。
研究結果表明,a-β 和 tau 蛋白的累積可能是疾病的結果,而不是最初的原因。這個想法可以幫助解釋早期理論中的缺陷。例如,細胞外部形成的斑塊可能不會直接影響細胞內部的 tau 蛋白或微管。
老化、蛋白質清除和新線索
該模型也與大腦的蛋白質回收系統隨著年齡的增長而減慢的證據一致。自噬作用通常會從細胞中去除α-β等蛋白質。當這個過程衰退時,a-beta 就會累積並與 tau 競爭進入微管。
其他研究也支持此觀點。一些研究表明,鋰可以降低阿茲海默症的風險,早期的研究表明,鋰有助於穩定微管。這表明加強這些結構可以限制 a-β 的有害影響。
如果得到證實,這些發現可能會改變阿茲海默症的治療方式。未來的療法可能不僅專注於去除蛋白質團塊,而是旨在阻止 a-β 幹擾微管或提高細胞清除微管的能力。
朱利安說,這項研究匯集了許多先前互不相關的發現。
「這個想法有助於理解許多以前看似無關的結果,」朱利安說。 “它讓我們更清楚地了解神經元內部可能出了什麼問題,以及新的治療可能從哪裡開始。”
參考文獻:“連接澱粉樣蛋白 β 和 tau 的微管關係:關於阿茲海默症根本原因的簡單而統一的理論”,作者:Thomas A Shoff、Maxence Derbez-Morin、Peishan Cai 和 Ryan R Julian,2026 年 3 月 17 日,美國國家科學院院刊.
DOI:10.1093/pnasnexus/pgag034
永遠不要錯過突破:
關注我們和谷歌新聞.
一項新的研究挑戰了長期以來的觀點:阿茲海默症主要是由澱粉樣斑塊驅動的,而不是指向神經元內部微妙但關鍵的競爭。
領導的新研究,顯示阿茲海默症可能不像人們普遍認為的那樣僅僅由大腦中斑塊的堆積引起。相反,它可能是由一種蛋白質破壞另一種蛋白質的正常功能引起的。
多年來,科學家一直將β澱粉樣蛋白(a-β)視為阿茲海默症的主要原因。這種蛋白質的簇常見於患者體內,而提高 a-β 水平的基因突變已知會引發早發性阿茲海默症。
然而,數以千計的旨在消除α-β的臨床試驗未能阻止或逆轉這種疾病。
研究人員也知道,另一種蛋白質 tau 蛋白會在阿茲海默症患者的大腦中累積。儘管如此,tau 蛋白和 a-beta 蛋白如何相互作用仍不確定。 「除了失智症之外,阿茲海默症的診斷還需要大腦中 a-beta 和 tau 蛋白的積累,」加州大學河濱分校化學教授兼研究主要作者 Ryan Julian 說。 “但許多實驗室只關注其中一個的作用而忽略另一個。”
這項新研究發表於美國國家科學院院刊顯示兩種蛋白質之間存在直接聯繫。
Tau 在穩定微管(細胞內結構)方面發揮關鍵作用。這些微小的管子就像運輸路線一樣,幫助在神經細胞中移動必需的分子。沒有它們,神經元就無法傳遞生存和溝通所需的物質。
神經元內部的競爭
研究團隊發現,tau 蛋白與微管結合的部分與 a-beta 的大小和形狀非常吻合。這種相似性表明 a-beta 也可能附著在這些結構上。
為了測試這一點,研究人員用螢光標記標記了 a-β。它的運動和光訊號的變化使他們能夠檢測到它何時與微管結合。
結果表明,a-β 和 tau 蛋白以相似的強度附著在微管上。這意味著當 a-beta 在神經元內部積聚時,它會將 tau 蛋白推離原來的位置。
Julian 說:“我們的工作表明,β 澱粉樣蛋白和 tau 蛋白會競爭微管上的相同結合位點,而 a-β 蛋白會阻止 tau 蛋白正常發揮作用。”
這種幹擾可能標誌著疾病的開始。當 tau 蛋白被取代時,細胞的內部運輸系統開始出現故障。同時,tau 蛋白可以開始聚集在一起並移動到神經元中不屬於它的部分。
研究結果表明,a-β 和 tau 蛋白的累積可能是疾病的結果,而不是最初的原因。這個想法可以幫助解釋早期理論中的缺陷。例如,細胞外部形成的斑塊可能不會直接影響細胞內部的 tau 蛋白或微管。
老化、蛋白質清除和新線索
該模型也與大腦的蛋白質回收系統隨著年齡的增長而減慢的證據一致。自噬作用通常會從細胞中去除α-β等蛋白質。當這個過程衰退時,a-beta 就會累積並與 tau 競爭進入微管。
其他研究也支持此觀點。一些研究表明,鋰可以降低阿茲海默症的風險,早期的研究表明,鋰有助於穩定微管。這表明加強這些結構可以限制 a-β 的有害影響。
如果得到證實,這些發現可能會改變阿茲海默症的治療方式。未來的療法可能不僅專注於去除蛋白質團塊,而是旨在阻止 a-β 幹擾微管或提高細胞清除微管的能力。
朱利安說,這項研究匯集了許多先前互不相關的發現。
「這個想法有助於理解許多以前看似無關的結果,」朱利安說。 “它讓我們更清楚地了解神經元內部可能出了什麼問題,以及新的治療可能從哪裡開始。”
參考文獻:“連接澱粉樣蛋白 β 和 tau 的微管關係:關於阿茲海默症根本原因的簡單而統一的理論”,作者:Thomas A Shoff、Maxence Derbez-Morin、Peishan Cai 和 Ryan R Julian,2026 年 3 月 17 日,美國國家科學院院刊.
DOI:10.1093/pnasnexus/pgag034
永遠不要錯過突破:
關注我們和谷歌新聞.